第三者認証審査
1.医療器申請の種類
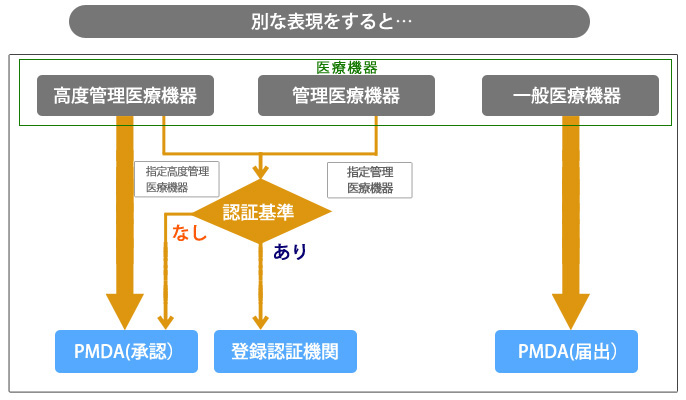
薬機法では医療機器の製造販売をしようとする者は、厚生労働大臣の承認を受けなければならず医療機器製造販売業者は医療機器の品目ごとに承認や認証の取得、又は届出が必要とされています。つまり医療機器は先に述べたクラス分類ごとに手続きと認可の方法が異なります。
認証申請とは厚生労働大臣が基準を定めて指定した指定管理医療機器及び指定高度管理医療機器に該当するものを指します。
(薬機法23条の2の5:承認、、23条2の23:認証、23条2の12:届出)
| 医療機器の区分 | 実施者 | |||
|---|---|---|---|---|
| 承 認 ・ 認 証 に 係 わ る 調 査 |
クラスⅡ | 認証 | 国内製造 | 登録認証機関 |
| 海外製造 | 登録認証機関 | |||
| クラスⅢ (新認証) |
国内製造 | 登録認証機関 | ||
| 海外製造 | 登録認証機関 | |||
| クラスⅢ (承認) |
大臣承認 | 国内製造 | PMDA | |
| 海外製造 | PMDA | |||
| クラスⅣ | 国内製造 | PMDA | ||
| 海外製造 | PMDA | |||
問題事案の発生等に伴う法69条に基づく立入検査等 ⇒ 都道府県 又は 国
第三者認証審査の現況
クラスⅡ・クラスⅢで指定高度管理医療機器あるいは指定管理医療機器に該当するものは、第三者認証機関へ認証申請することになります。現在、薬機法第23条の6第1項の規定により登録されている第三者認証機関は13機関となっています。また各機関により認証業務の範囲が異なるほか、同様の認証業務であっても審査費用と審査内容にはバラツキがありますので十分に確認しましょう。さらに、JIS規格への適合性試験が必要になる場合があることにも注意が必要です。
医療機器は品目ごとに届出、認証、承認の手続きが必要となります。必要な手続きは医療機器のクラス分類に応じて異なり、申請先も異なれば必要な期間・費用も異なるので注意が必要です。

