リスク分析
医療機器に要求される 『リスクマネジメント』
様々な生活上のシーンでリスクマネジメントが叫ばれていますが、医療機器も例外ではありません。医療機器はその性格上、あらかじめリスクを想定し対策を講じておくことが必要であり、JIS T 14971等でリスクマネジメントの要求をされています。
医療機器のリスクマネジメントとは、医療機器のリスクを管理するための枠組みであり、①リスク分析、②リスク評価、③リスクコントロール、④製造中および製造後情報のレビューを含んだプロセスであり、管理方針、手順および実施を体系的に適用することとあります。
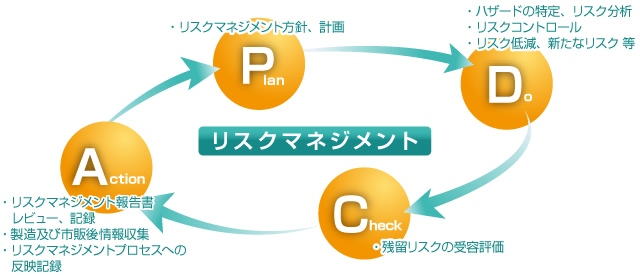
つまり医療機器では、患者、使用者が危険に遭わないように事前にその原因となるものを低減しておくことに加え、そのリスクを管理する手順も含めることがリスクマネジメントということになります。JIS T 14971では製造販売業者が行う承認申請や認証申請時にリスクマネジメントに関する資料の添付が要求されています。具体的には、設計や開発の段階から製造、市販後にいたる全てのプロセスにおいて、リスクの分析→リスクの評価→リスクのコントロール→残留リスク全体の受容可能性評価→リスクマネジメントのプロセスをレビュー→製造及び市販後情報の反映、といった活動を実施しPDCAサイクルとしていくことになります。
医療機器のリスクマネジメントは患者、使用者になった気持ちで取り組むことが最初の第一歩です。さらに、製品申請前、QMS調査申請前に当局からの安全対策通知、類似品の不具合情報を入手して、添付文書、取扱説明書の改訂等によるリスクマネジメントの実施、さらに開発・製造部門(業者)へ再度リスクマネジメントの実施を促すことが大切です。
医療機器は生体に影響を与えるリスクが大きいので、リスクマネジメントを徹底するようJISで定められています。設計段階、開発段階はもちろんのこと、製造・市販後にいたる全てのプロセスにおいて、情報を収集し改善を行うというPDCAサイクルを回していくことが求められています。
